电子数据采集英文简称EDC,英文全称Electronic Data Capture,相对于纸质版的传统CRF,EDC更适合临床研究信息管理的自动化
定义
电子数据采集是一种基于计算机网络的用于临床试验数据采集的技术,通过硬件、软件、人员和SOP的有机结合,以电子化的形式直接采集和传递临床数据。
An Electronic Data Capture (EDC) system is a computerized system designed for the collection of clinical data in electronic format for use mainly in human clinical trials. EDC replaces the traditional paper-based data collection methodology to streamline data collection and expedite the time to market for drugs and medical devices
ICH-GCP E6中的表述:
When using electronic trial data handling and/or remote electronic trial data systems, the sponsor should:
应用电子试验数据处理和/或遥控电子试验数据系统时,申办者应当:
Ensure and document that the electronic data processing system(s) conforms to the sponsor’s established requirements for completeness, accuracy, reliability, and consistent intended performance (i.e. validation).
确保并证明电子数据处理系统符合申办者所设定的关于完整性、准确性、可靠性和一致期望的性能(如数据确认)的要求。
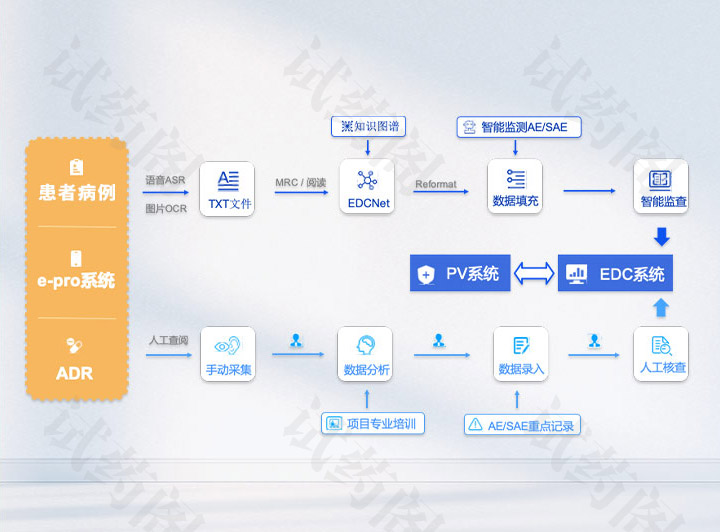
药物临床试验质量管理规范2020版中的表述:
第三十六条 申办者在试验管理、数据处理与记录保存中应当符合以下要求:
(三)申办者使用的电子数据管理系统,应当通过可靠的系统验证,符合预先设置的技术性能,以保证试验数据的完整、准确、可靠,并保证在整个试验过程中系统始终处于验证有效的状态。
(四)电子数据管理系统应当具有完整的使用标准操作规程,覆盖电子数据管理的设置、安装和使用;标准操作规程应当说明该系统的验证、功能测试、数据采集和处理、系统维护、系统安全性测试、变更控制、数据备份、恢复、系统的应急预案和软件报废;标准操作规程应当明确使用计算机化系统时,申办者、研究者和临床试验机构的职责。所有使用计算机化系统的人员应当经过培训。
(五)计算机化系统数据修改的方式应当预先规定,其修改过程应当完整记录,原数据(如保留电子数据稽查轨迹、数据轨迹和编辑轨迹)应当保留;电子数据的整合、内容和结构应当有明确规定,以确保电子数据的完整性;当计算机化系统出现变更时,如软件升级或者数据转移等,确保电子数据的完整性更为重要。
若数据处理过程中发生数据转换,确保转换后的数据与原数据一致,和该数据转化过程的可见性。
(六)保证电子数据管理系统的安全性,未经授权的人员不能访问;保存被授权修改数据人员的名单;电子数据应当及时备份;盲法设计的临床试验,应当始终保持盲法状态,包括数据录入和处理。
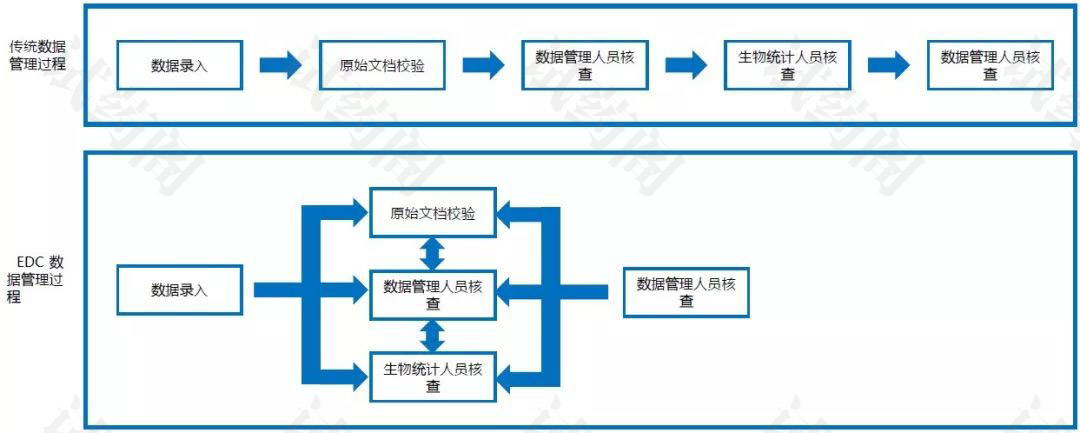
EDC系统的优点
- 提高了临床研究的效率,缩短了临床研究周期;
- 通过逻辑检验和录入数据检查提高了数据质量;
- 对研究质量的监测更加方便。
EDC系统的功能
- 数据录入:包括二次录入、逻辑检验、录入数据控制(如必填项、日期、有效值验证)、电子签名(即满足FDA 21 CFR Part 11要求)
- 数据导出:可导出多种格式,例如Excel、SPSS、SAS等等,有时还需要导出用于数据交换的CDISC ODM的xml格式
- 试验设计:包括eCRF设计、事件设计(如筛选期、基线期和随访期)、受试者分组等等
- 数据核查:包括源数据核查SDV、自动和手工质疑的产生和解答
- 稽查:稽查痕迹
- 系统安全:包括使用https进行数据传输,数据库定期备份,基于角色的权限控制(如数据管理员、申办者、监查员、研究者、CRC等等),数据库锁定与解锁
- 支持多中心
- 随机化:支持多种随机化方法,如简单随机化、分层区组随机化、动态随机化
- 医学编码:支持字典MedDRA、WHO DD等等
- 支持多语言:进行国际化的药物临床试验必不可少

EDC系统的选择
国外EDC系统有:甲骨文(Oracle)的OC-RDC、Medidata的Rave
国内EDC系统有太美医疗等,一套EDC系统的市场均价约为10万元-15万元

 关注微信公众号
关注微信公众号
