SAE(Serious Adverse Event,严重不良事件)是指在临床试验过程中发生的严重不良反应,它可能对试验受试者的健康造成威胁,甚至导致死亡。SAE的报告是临床试验过程中必须严格遵守的法律和伦理要求之一,它是确保试验安全性的重要步骤。
SUSAR(Suspected Unexpected Serious Adverse Reaction,可疑且非预期严重不良反应 ):是指一种严重的、预期之外的疑似不良反应。这种反应可能与临床试验药物相关,但与该药物已知的安全性资料不符合。在药物临床试验中,SUSAR是一种重要的安全事件,需要及时报告,并进行处理,以确保试验的安全性和可靠性。
一、临床试验SAE报告的流程:
- SAE发生:在临床试验过程中,如果试验受试者出现严重不良反应,研究人员应该立即采取措施保护患者的生命安全,并停止试验。
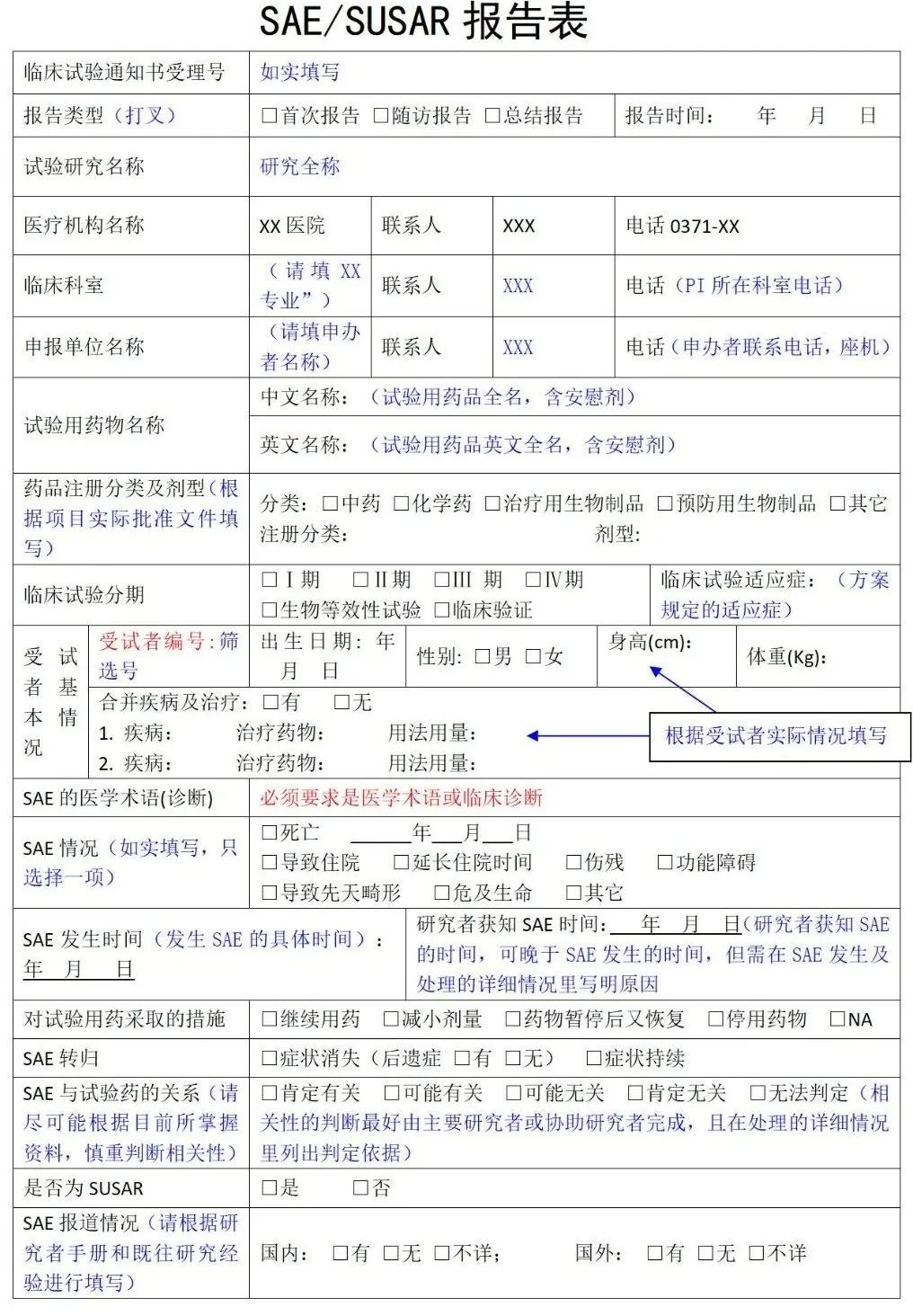
- 报告准备:研究人员应该立即填写SAE报告表格,并尽快向研究伦理委员会和监管机构报告。SAE报告表格通常包括试验受试者的个人信息、SAE的描述、发生时间、严重程度、与试验药物的关联性、治疗情况和结果等信息。
- 伦理委员会审查:研究人员应该尽快向研究伦理委员会报告SAE。伦理委员会会审核SAE报告,并决定是否需要停止试验或者对试验进行调整。如果伦理委员会认为试验安全性有问题,它可以要求研究人员停止试验或者对试验进行调整。
- 监管机构审查:研究人员还应该向监管机构报告SAE。监管机构会审核SAE报告,并决定是否需要采取进一步行动,例如停止试验或者撤销试验批准。
- 事后处理:如果试验受试者在试验过程中发生SAE,研究人员应该对试验受试者进行充分的事后处理,包括提供紧急治疗和跟踪观察,以便及时发现和处理可能出现的后遗症。
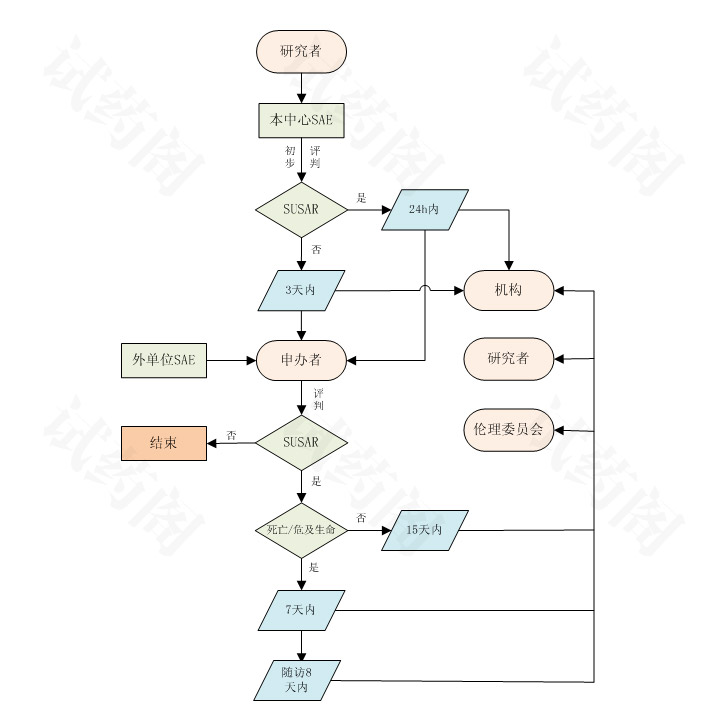
SAE报告实际操作:
1. 申办者向我院递交的资料(如研究方案或其他文件),应包括研究者向申办者报告SAE的途径和要求等内容。
2. 研究者在获知SAE后应及时向申办者报告,并初步分析是否为SUSAR。如是SUSAR,要求在24h内报告;非SUSAR的其他SAE,要求3天内或按照研究方案的要求报告。研究者提交给申办者的SAE报告,须按照我院统一模板进行书写,并同步抄送给药物临床试验机构办公室(安全性事件报告专用邮箱为XX@163.com),妊娠事件按照SAE流程进行报告,研究者还需将附件严重不良事件登记表发送至邮箱。
二、SUSAR报告流程
SUSAR的报告和处理流程是:
- 临床试验中的调查员、研究者或参与者应及时发现并报告SUSAR。
- 报告SUSAR后,主要负责人应立即采取适当的措施,确保受试者的安全。
- 报告SUSAR后,主要负责人应将SUSAR报告提交给监管机构和伦理委员会,并与药品研发者进行沟通,以共同制定适当的安全措施。
- 监管机构和伦理委员会应及时审核和处理SUSAR报告,并根据情况决定是否需要终止临床试验。
- 药品研发者应根据监管机构和伦理委员会的决定,制定相应的安全管理计划,以保证试验的安全性和可靠性。
SUSAR报告实际操作:
1. 申办者收到研究者报告的SAE等安全性相关信息后,判读是否是SUSAR。申办者评估与研究者判读结果不一致时,应说明理由,并要求按SUSAR快速报告。
2. 申办者将确定的SUSAR报告电子版发送给主要研究者、药物临床试验机构办公室(XX@163.com)、伦理委员会办公室(XX@163.com)。致死或者危及生命的SUSAR,申办者应在首次获知后尽快报告,但不得超过7天,并在随后的8天内报告、完善随访信息(以申办者获知事件为0天计算)。非致死或者危及生命的SUSAR,申办者应在首次获知后15天内尽早报告给各部门。
3. 研究者、药物临床试验机构办公室、伦理委员会办公室及时签收申办者提交的SUSAR等安全性资料。
4. 研究者和伦理委员会根据申办者提供的SUSAR等安全性资料,应衡量继续开展试验的风险和获益,如受试者继续参与试验的风险/获益比明显增高,应考虑采取及时和恰当的措施保护受试者安全和权益。
三、其他情况
如受试者完成治疗或疾病进展后发生的任何符合SAE定义的情况,原则上不作为SAE上报;但研究方案中有特殊规定,则按照研究方案执行;

总之,SAE报告是临床试验过程中非常重要的一环,它可以帮助研究人员及时识别并处理试验中的风险,保护试验受试者的生命安全。在SAE报告过程中,研究人员应该及时报告,严格遵守相关规定,确保试验的安全性和科学性
参考文献:1.《药物临床试验质量管理规范》2.《药物临床试验期间安全性数据快速报告标准和程序》3.《研发期间安全性更新报告要求及管理规定》

 关注微信公众号
关注微信公众号
